El presidente Andrés Manuel López Obrador informó este viernes que la Comisión Federal para la Protección contra Riesgos Sanitarios (Cofepris) autorizó el uso de emergencia controlado de la píldora para combatir el Covid-19 de la farmacéutica Merck & CO.
“Hay además ya dos medicamentos que se están aprobando, están en proceso de aprobación por Cofepris que resultan efectivos, tomados y ya están por autorizarse y se van a empezar a aplicar en hospitales públicos, para que estén al acceso de todos”.
Sobre estas dos opciones AMLO también señaló que una vez se aprueben comenzarán a utilizarse en hospitales públicos, con la intención de que sean accesibles para todas las personas.
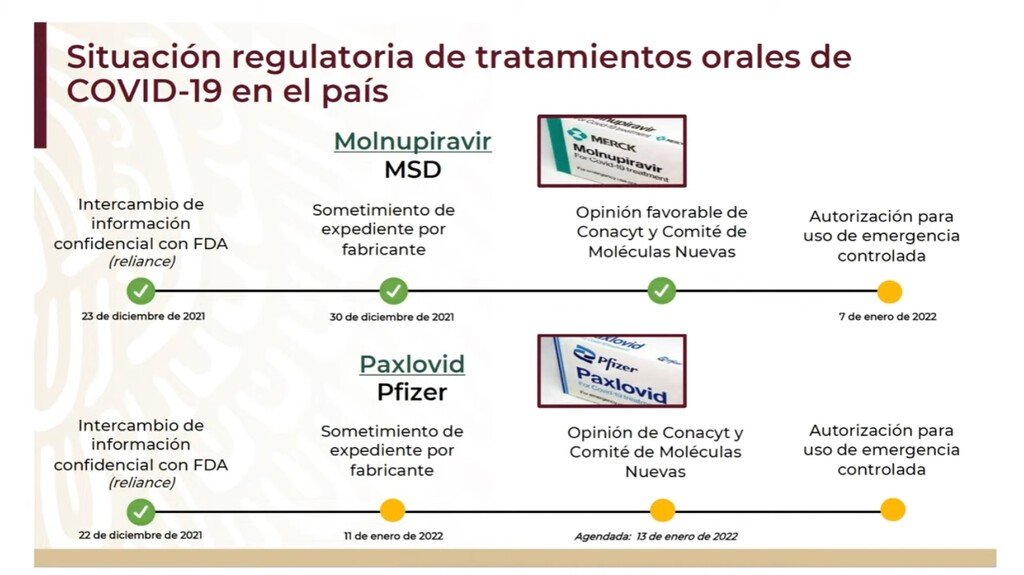
En el caso de Merck, se espera que la autorización para el uso de emergencia del medicamento Molnupiravir se de este viernes 7 de enero, mientras que la revisión del Paxlovid de Pfizer será hasta el miércoles 12 de enero, por lo que todavía estaría pendiente su aprobación.
Merck: servirá para tratar la enfermedad por coronavirus leve a moderada 2019 (COVID-19) en adultos con resultados positivos de pruebas virales directas de SARS-CoV-2, y que son en alto riesgo de progresión a COVID-19 grave, incluida la hospitalización o la muerte, y para quienes las opciones de tratamiento alternativo de COVID-19.
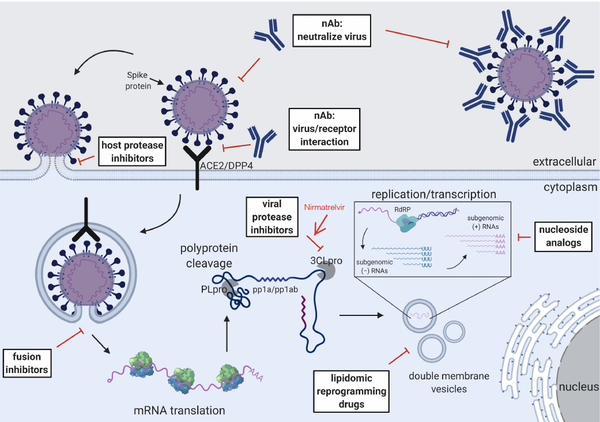
Paxlovid: es un antiviral actúa inhibiendo la proteasa 3C (3CLPRO), también conocida como MPRO. Esta es la principal enzima que participa en la maduración proteolítica del coronavirus, mediando en la escisión de las poliproteínas PP1a y PP1ab.
El presidente de México también informó que hasta el momento se está analizando cómo se adquirirán estos medicamentos y cuál será el número de dosis una vez que las autoridades regulatorias del país den el visto bueno.